Curentul electric in electroliti
Electrolitii sunt soluții de substanțe sau se topește, care conduce curentul electric.
Prin electrolitii includ săruri, acizi și baze.
Pentru electrolitul având sarcini libere. este necesar să se dizolve sau topi.
O disociere electrolitica - o descompunere a moleculelor de electrolit în ioni sub influența solventului. Astfel au format ionii pozitivi și negativi, care sunt purtători în electroliți.
Procesul de trecerea unui curent electric prin electrolit însoțită de transformări chimice și separarea substanței pure la electrozi, numit electroliza.
In electroliza, ionii pozitivi se miște spre substanța negativă
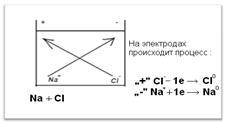
electrod telnomu (catod). și negativ la pozitiv (anod). Urcarea electrodul, ei fie dau excesul de electroni, sau de a dobândi sub-stayuschie și formează un compus neutru.
legea lui Faraday de electroliză: m = k q = k I # 916; T
Greutatea substanței pure, a evoluat la electrod, ca urmare a electro-sis, este direct proporțională cu cantitatea de energie electrică care curge prin soluție.
unde k - factorul de proporționalitate - substanță echivalentă electrochimice.
Utilizarea electrolizei în domeniu. obținut prin electroliza topit metale ușoare minereu care reacționează cu apă și nu se disting de soluții. Prin electroliza produce un strat de obiecte din metal-ically strat subțire de alt metal. Cu electroliza puteți obține de relief copie de metal-Nye. Electroliza este utilizat pe scară largă în celulele electrochimice.